近日,一组来自华大生命科学研究院、中国科学院等顶级科研单位的科学家们在《自然》杂志上发表了一项研究,宣布发现了一种无转基因、快速、可控的方法,可以将多能干细胞转化为真正的8细胞全能胚胎样细胞,为器官再生研究和合成生物学的进步铺平了道路。

网页截图
研究团队在华大基因单细胞测序技术协助下,将多能干细胞(即早期胚胎细胞的“成年”版本)转化为更“年轻”的细胞,这些细胞具有人类受精卵基因组的激活状态,并保留各种细胞谱系发展的潜力。
这些细胞有望在未来用于人体患病器官的再生,进而降低世界对器官移植的依赖。它们也可以用来生成人造囊胚。此外,它们还将有助于研究人类胚胎发育,帮助治疗早期发育相关得疾病,并防止流产。
虽然将多能干细胞转化为囊胚内的内细胞团样细胞的技术早就有,但这项研究是首次将多能干细胞转化为人类发育周期中与8细胞胚胎相匹配的真正早期阶段,这将有助于增加人们对早期人类胚胎发育的认识。至关重要的是,转换后的细胞可以在体内生成胎盘细胞——这是目前世界首次完成的成果。
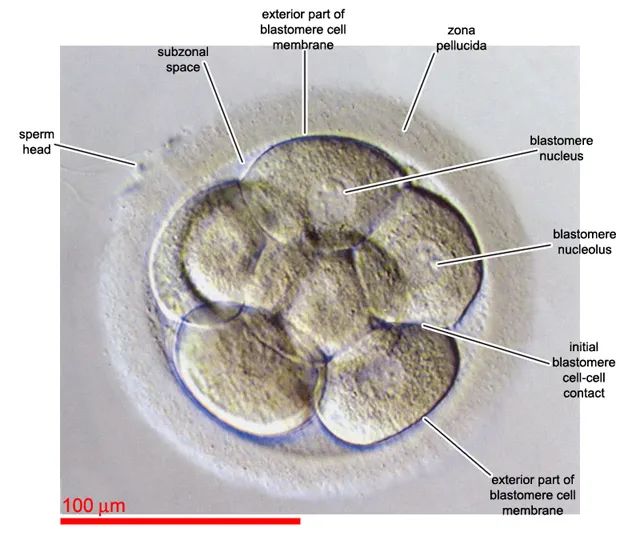
8细胞胚胎 | 参考文献[3]
“全能8细胞阶段的胚胎样细胞只经过3次分裂就重现受精卵的胚胎状态。与已报道的多能干细胞相比,这些细胞不仅能分化成胎盘组织,还有发育成更成熟的器官的潜能,这对于全世界数百万等待器官移植的患者来说是个好消息。” 论文的通讯作者 Miguel A. Esteban 教授、Md. Abdul Mazid 博士和中国科学院的李文娟博士解释说。
“这一突破也是再生医学和单细胞测序技术结合的一个完美例子。” 论文的另一位通讯作者、华大生命科学研究院的刘龙奇博士说,“通过大规模的单细胞多组学分析,加上干细胞技术对在体外或体内获得的细胞或组织的高效与准确的鉴定,都将大大推进再生医学的研究。”
处于早期发育阶段的细胞可以被称为全能细胞,这意味着它们有潜力创造出所有类型的早期胚胎细胞,而这些早期胚胎细胞又发展出个体发育所需的组织和器官。这项研究建立在之前对囊胚阶段多能干细胞的研究基础上,囊胚阶段的细胞有潜力创造出分化的细胞和组织。
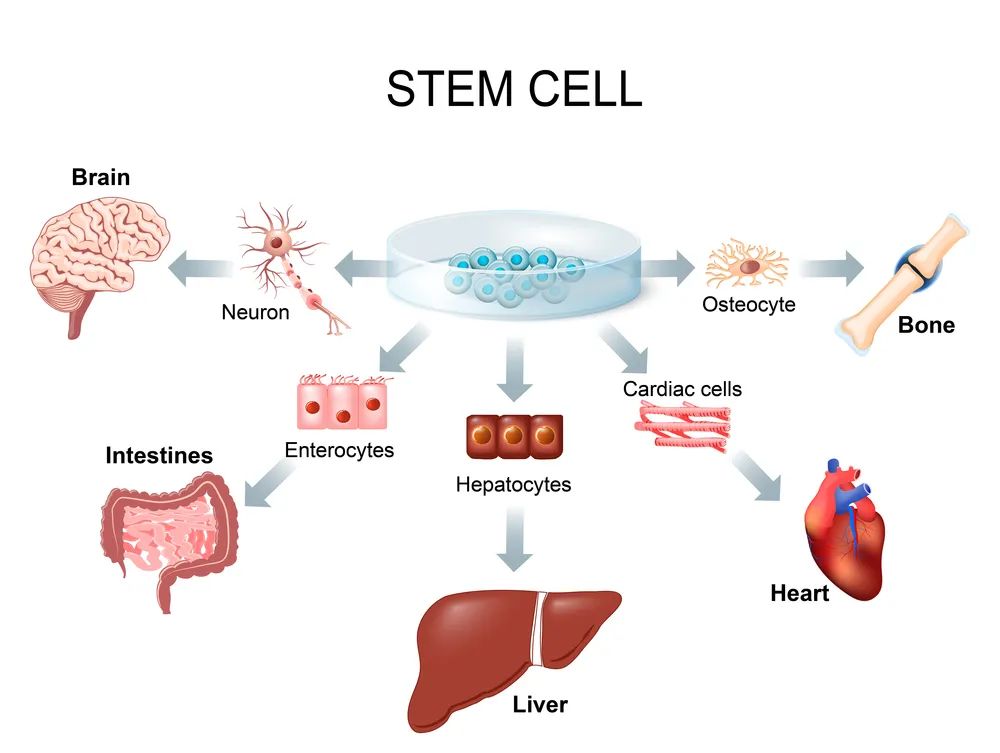
干细胞分化 | 站酷海洛
这项研究的突破是基于单细胞测序技术的进步,华大基因集团在这一领域处于世界领先水平。其单细胞文库测序平台,结合其测序技术,使大量的和多维的单细胞分析具有高灵敏度和高准确性,同时具有低成本的优势。
这项研究背后的国际团队提取了多能干细胞,并用鸡尾酒试剂对其进行处理,才制造出这样的8细胞胚胎样细胞。在其他实验中,这些细胞被分类并注射到老鼠体内进行进一步发育,然后使用华大基因的单细胞基因组分析进行分析。这项创新技术有助于科学家识别和分离8细胞胚胎样细胞,并证明其在生物体内产生胎盘细胞的能力。

这些细胞被分类并注射到老鼠体内进行进一步发育 | Flickr,audrey_sel / CC BY-SA 2.0(https://creativecommons.org/licenses/by-sa/2.0/)
研究人员所取得的进展最终可能使个性化的器官再生成为现实。通常,对于那些需要器官移植的人来说,唯一可行的方法就是找到一个匹配的捐赠者。这个过程并不是万能的。如果供者血清型与受者血清型太不同,移植可能会失败。另一项旨在通过基因编辑使动物器官适应人类移植的程序也处于初级阶段。
这一成果也为研究早期胚胎发育提供了一个新的体外研究系统,有助于我们了解早期胚胎发育与疾病发生之间的关系,为研究治疗出生缺陷和各种发育疾病提供了资源。
参考文献
[1] Mazid, M.A., Ward, C., Luo, Z. et al. Rolling back of human pluripotent stem cells to an 8-cell embryo-like stage. Nature (2022). https://doi.org/10.1038/s41586-022-04625-0
[2] https://www.eurekalert.org/news-releases/947096
[3] Veeck, L.L., and Zaninović, N. 2003. An atlas of human blastocysts. Parthenon Publishing Group, New York.
复制本文链接 文章为作者独立观点不代表本网站立场,未经允许不得转载。

 京公网安备
11010802036058号
京公网安备
11010802036058号
评论