糖尿病是全球增长最快的代谢疾病,预计到2045年将影响约6.93亿人的健康。大血管疾病(动脉粥样硬化和心脏病)和微血管疾病(肾病、视网膜病和神经系统疾病),是糖尿病引起的最常见的并发症。如心力衰竭、中风、静脉和动脉血栓形成、心肌病和视力障碍,是导致心血管疾病的高风险诱因。内皮损伤是大多数血管并发症的主要早期问题,高血糖严重抑制内皮细胞活力,加速内皮细胞凋亡和衰老。
迄今为止,针对糖尿病血管并发症的药物很少,常用的药物如双胍类(二甲双胍)、磺脲类、噻唑烷二酮类(格列酮类)、格列奈类(glinides)和α-葡萄糖苷酶抑制剂,但仅是间接靶向血糖稳态,修复血管损伤。而且这些药物在临床上仍存在副作用,因此,需要新的方法来专门针对糖尿病的血管并发症。
目前,基于间充质干细胞 (MSCs) 的细胞疗法已被公认为治疗糖尿病及其并发症等多种疾病的有效方法。MSCs具有归巢和旁分泌能力,能够迁移到受损组织部位并释放细胞外囊泡、生长因子、趋化因子和细胞因子,从而调节免疫反应并修复受损组织。例如,间充质干细胞分泌生长因子(bFGF、IGF-1、HGF和VEGF等)刺激细胞增殖和组织修复;分泌抗炎因子(IL-10和IL1-RA)抑制局部炎症;分泌外泌体和细胞外RNA触发细胞间通讯和调节。临床研究表明,输注MSCs的糖尿病患者的餐后血糖和HbA1水平显著降低。
此外,间充质干细胞通过改善血管生成、减少氧化应激损伤和巨噬细胞浸润、加速组织修复和再生,在治疗糖尿病并发症(如视网膜病变、肾病和足部溃疡)方面具有治疗潜力 。因此,间充质干细胞疗法是治疗糖尿病及其并发症的一种有前途的方法。
近日,Stem Cell Research & Therapy杂志报道了间充质干细胞在修复糖尿病血管损伤中的作用,并且首次揭示人脐带间充质干细胞(hucMSCs)对受损内皮细胞的旁分泌作用方式,发现了MAPK/ERK信号通路介导的人脐带间充质干细胞修复内皮的机制。

考虑到MSCs的组织修复和促血管生成能力,研究者提出了一个假设,即MSCs可以通过旁分泌作用恢复糖尿病引起的血管内皮损伤。为了验证这一点,他们采用人脐带间充质干细胞(hucMSCs)治疗大鼠糖尿病模型和在人内皮细胞(HUVECs)模型进行研究,探讨了间充质干细胞对糖尿病内皮损伤的疗效和旁分泌机制。该研究结果为hucMSCs治疗糖尿病血管并发症提供了新的认识,表明间充质干细胞是临床细胞治疗的理想来源。
o1 动物体内研究
为了评价人脐带间充质干细胞对血糖和血管内皮功能的治疗作用,在注射细胞之前和注射细胞之后(1、2、3、4周)每周监测糖尿病大鼠的体重和FBG。在细胞治疗4周后(最后一次注射后7天)检测了ICAM-1(细胞间黏附分子)和VCAM-1(血管细胞间黏附分子)的血液水平。模型组ICAM-1、VCAM-1水平显著高于对照组,VCAM-1水平显著恢复到正常水平。

高、低剂量人脐带间充质干细胞移植后,主动脉内皮组织学形态明显改善,内膜光滑完整,内皮细胞恢复。此外,图B显示模型大鼠的平均内皮厚度显著高于正常大鼠,证实细胞治疗组均显著恢复。免疫组化结果显示,模型组p-ERK和HH3阳性棕色信号明显改变,细胞治疗促进其恢复。
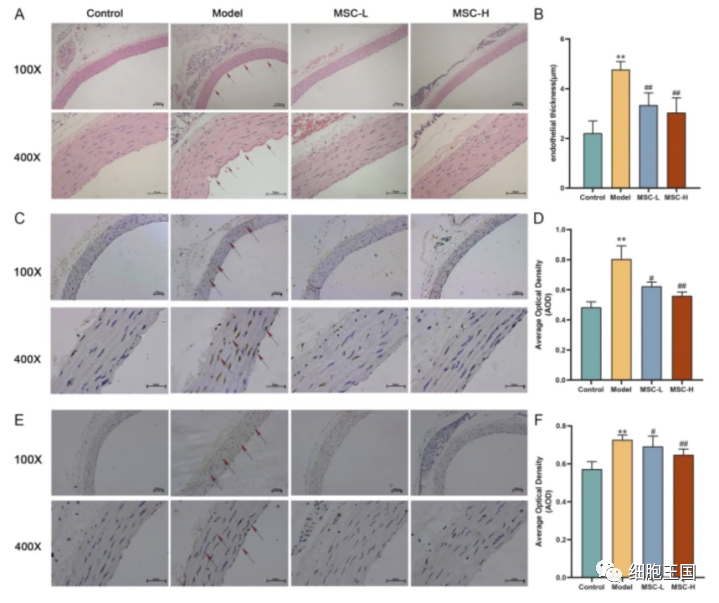
hucMSCs对糖尿病引起的主动脉内皮组织病理学改变的影响。
为了确定间充质干细胞对上皮细胞的旁分泌作用,研究者评估了细胞治疗组的细胞活力、伤口愈合和 transwell 迁移。图 A、B中,模型组荧光强度明显低于对照组,而细胞治疗组荧光强度明显恢复正常水平。模型组内皮细胞的 transwell 迁移明显受到抑制,而间充质干细胞治疗组的内皮细胞的 transwell 迁移明显恢复正常。
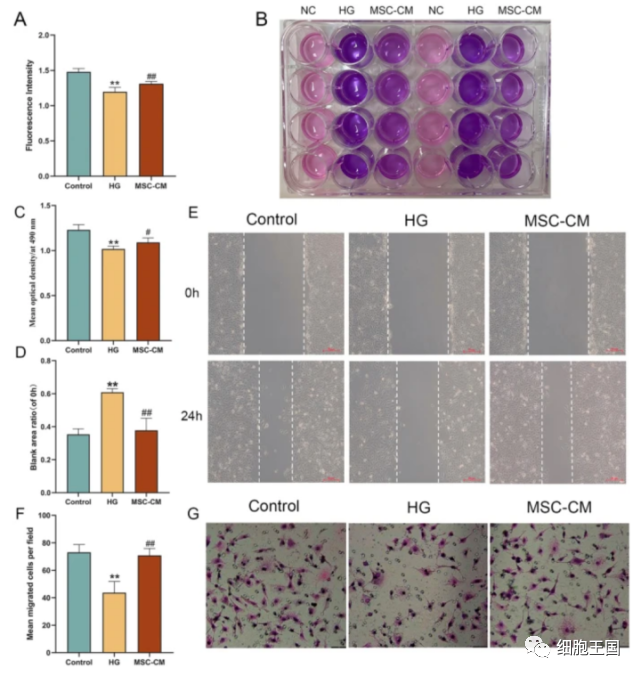
MSC对HUVEC细胞活力、伤口愈合和细胞迁移的影响。
与对照组相比,内皮细胞的管形成被严重破坏,间充质干细胞对其发挥了疗效。对糖尿病内皮细胞小管网络的形成起到了旁分泌作用。
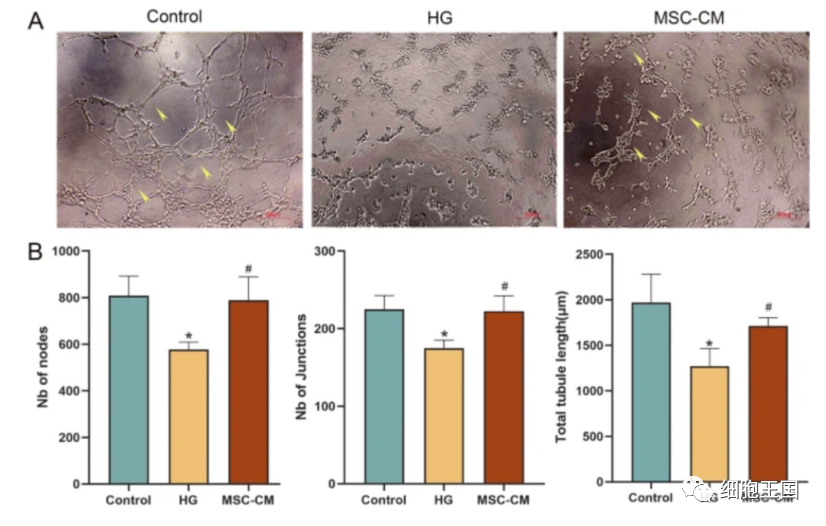
hucMSCs对HUVECs小管形成的影响
检测细胞衰老(P16、P53、BAX、IL-6、TNF-α)和管状形成(ET1、ICAM-1、VCAM-1)相关基因的mRNA表达,分析细胞治疗对处于高血糖状态的内皮细胞的分子调控。发现,高血糖显著上调了这些基因的mRNA表达,而间充质干细胞有效地恢复了改变,表明其对糖尿病造成的内皮细胞衰老和管形成抑制具有积极的分子作用。
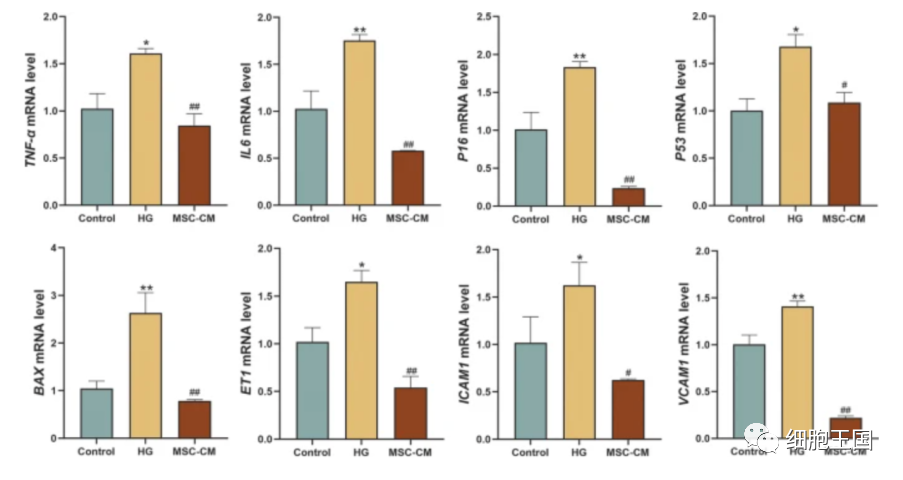
mRNA在对照组、模型组和MSC组中表达HUVECs细胞衰老和管形成相关基因。
在共培养条件下进行了细胞活力测定、伤口愈合 transwell 测定和 PCR。模型组的细胞活力明显低于对照组,而 MSC 治疗组的细胞活力显着提高。图B、C中,模型组创面愈合能力明显受到抑制,而MSC治疗组恢复正常。在图D、E,模型组内皮细胞 transwell 迁移明显受到抑制,MSC治疗组内皮细胞transwell迁移明显恢复正常。在图F中,模型组炎症( IL6、TNF-α)、迁移(ET1)和细胞凋亡(BAX)的 mRNA 表达水平显着上调,而MSC组显著逆转。进一步证实了旁分泌作用。
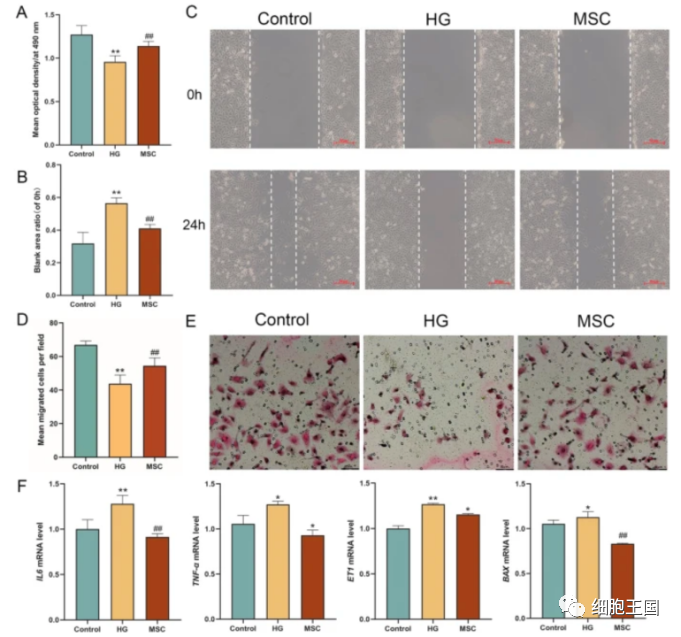
共培养条件下hucMSCs对HUVECs细胞活力、伤口愈合、细胞迁移和mRNA表达的影响。
o2 观点和结论
糖尿病血管并发症是糖尿病患者最常见的死亡原因,可导致大血管(动脉粥样硬化和心脏病)和微血管(肾病、视网膜病和神经病)疾病。内皮损伤或功能障碍在糖尿病血管并发症过程中起初步作用,表现为血管收缩因子分泌增加、内皮细胞受损、内皮通透性紊乱、血栓形成紊乱等。例如,由于慢性炎症、白细胞增多、氧化应激和细胞因子失调引起的糖尿病视网膜病变早期,内皮细胞受到严重损伤,进一步导致周细胞减少,视网膜毛细血管形成无细胞毛细血管,血管通透性增加,并破坏内部血视网膜屏障。此外,糖尿病引起的内皮损伤可通过诱导结节性肾小球硬化、肾小球基底膜增厚和系膜扩张而引发肾病,最终导致肾小球滤过率下降。
内皮细胞衰老在糖尿病心血管疾病(如动脉粥样硬化)的发展中起关键作用,表现为细胞外观增大、炎症分泌和 SA-β-gal 活性增强、衰老相关基因和蛋白质表达增加等特征。因此,内皮损伤可作为糖尿病血管并发症治疗的重要靶点。在本研究中的数据表明,人脐带间充质干细胞不仅可以改善血糖,还可以通过改善内皮细胞的细胞活力、伤口愈合能力、迁移、衰老和炎症状态以及血管生成来修复内皮的糖尿病损伤,其中MAPK/ERK信号介导其分子旁分泌作用机制(下图)。
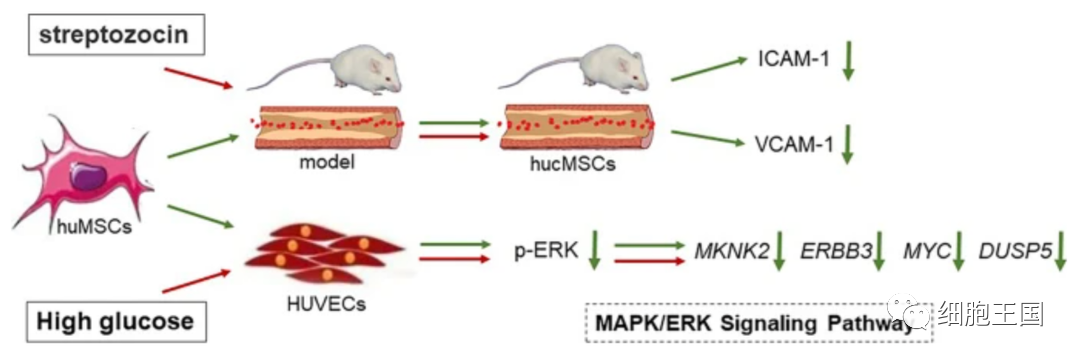
hucMSCs 改变葡萄糖对内皮细胞损伤的负面影响的机制。
红色箭头代表高糖诱导的损伤过程,绿色箭头代表 MSCs 干预过程
间充质干细胞已被广泛研究用于治疗糖尿病,很多临床研究对其血糖调节作用进行了评估。本文是第一项报道人脐带间充质干细胞对糖尿病血管内皮损伤的功效的研究。体内数据表明,人脐带间充质干细胞改善了糖尿病大鼠的高血糖和体重,并在组织病理学和血管功能方面修复了受损的血管内皮。体外数据进一步证实,人脐带间充质干细胞通过旁分泌作用改善了高葡萄糖损伤的内皮细胞的细胞活力、伤口愈合、迁移、血管生成和细胞衰老状态。
参考文献
1.Human umbilical cord-derived mesenchymal stem cells not only ameliorate blood glucose but also protect vascular endothelium from diabetic damage through a paracrine mechanism mediated by MAPK/ERK signaling.Stem Cell Research & Therapy volume 13, Article number: 258 (2022)
复制本文链接 文章为作者独立观点不代表本网站立场,未经允许不得转载。

 京公网安备
11010802036058号
京公网安备
11010802036058号
评论