胚胎干细胞(Embryonic stem cell,简称ESC)是一类具有多能性的干细胞。在卵细胞受精后,受精卵经过桑葚胚阶段,进入囊胚阶段。囊胚中的细胞可以归入两个大类:滋养层(trophoblast,TE)和内细胞群(inner cell mass,ICM)。滋养层的细胞会分化为胚胎外的组织(胎盘等),内细胞群的细胞则会分化成胚胎的其余结构。分离内细胞群细胞并进行体外(in vitro)培养,即可取得胚胎干细胞。胚胎干细胞拥有分化为三个胚层的细胞的潜能,或者说在一般情况下能分化形成除了胎盘之外的所有胚胎结构,此为胚胎干细胞多能性的具体体现。
1981年,英国剑桥大学遗传学部中,两个分别由马丁·埃文斯(Martin Evans)以及马修·考夫曼(Matthew Kaufman)率领的研究团队分别在体外建立了小鼠胚胎干细胞系。而胚胎干细胞这一术语则是由加州大学旧金山分校(UCSF)解剖学部的教授盖尔·马丁(Gail R. Martin)于当年12月的一篇论文中首次提出[2]。1998年,威斯康星大学教授詹姆斯·汤姆森(James Thomson)等人成功建立了人胚胎干细胞系。2007年,马丁·埃文斯与另外两名科学家因“利用胚胎干细胞引入特异性基因修饰的原理上的发现”而获得当年诺贝尔生理学或医学奖。
胚胎干细胞被认为在再生医学、组织工程、药物实验等领域拥有广阔的应用前景,胚胎干细胞对发育生物学的基础研究也有很大助益。但是,因为道德、宗教与法律上的问题(比如目前分离胚胎干细胞的方法会无可避免地杀死胚胎),有关胚胎干细胞的研究(即治疗性克隆)在各国都受到了一定的限制。
性质与特征
胚胎干细胞来自囊胚的内细胞群(ICM),并进行体外(in vitro)培养取得。胚胎干细胞具有多能性,在一定条件下能够分化为三个胚层(外胚层、中胚层、内胚层)的细胞,形成生物体的各种结构。胚胎干细胞的形态与基因表达情况与其他细胞有明显的不同。
形态学
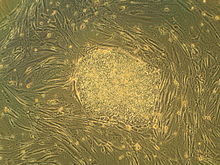
胚胎干细胞为球状,人胚胎干细胞直径约为14μm,而鼠胚胎干细胞直径约为8μm。胚胎干细胞的细胞核一般较大,核仁明显,而细胞质相对较少。人和小鼠的胚胎干细胞都能在培养皿上形成圆形、边界清晰、表面光滑的细胞集落。
分子细胞生物学
胚胎干细胞多能性的维持依赖于Sox2、Oct4、Nanog等因子构成的转录网络,确保与细胞自我更新能力有关的基因能够持续高水平表达,并抑制与分化、自噬相关的基因转录。在胚胎干细胞的分化过程中,细胞的基因表达情况会发生很大变化,尤其是与胚胎干细胞自我更新能力维持有关的基因。
胚胎干细胞的自我更新和分化与表观遗传学途径有密不可分的联系。首先是组蛋白的化学修饰:在胚胎干细胞中,与自我更新相关的基因所在区域组蛋白H3K27高度乙酰化,这些区域中既有组蛋白乙酰基转移酶,也有去乙酰化酶。这两种作用效果完全相反的酶使H3K27的乙酰化水平维持动态平衡,便于基因能在外界信号发生改变时迅速关闭。另外,PRC1与PRC2两种重要的蛋白质会使H3K27、H3K4发生甲基化而沉默与分化相关的基因,使其不表达。胚胎干细胞多能性的维持与RNA干扰也有紧密联系。比如,PRC1与PRC2还会沉默编码与分化相关的miRNA,使胚胎干细胞维持多能性;而let-7(一种miRNA)的表达则会使胚胎干细胞开始分化。受精卵发育早期,基因组所有的DNA甲基化都会由甲基转移酶Dmnt1消除;而与胚胎干细胞自我更新有关的基因区域会在分化过程中再次甲基化,这些基因的表达也随之停止。
胚胎干细胞多能性的维持还需要依靠胞外微环境提供适宜的信号,否则,胚胎干细胞很容易分化为其他类型的细胞。过去,胚胎干细胞的培养需要在有一层喂养层细胞的培养基上进行。喂养层细胞一般是经丝裂霉素等有丝分裂阻断剂处理过的胚胎成纤维细胞,这些细胞能分泌特定的信号分子模拟早期胚胎发育的微环境,使胚胎干细胞维持不分化的状态。目前,在培养基内加入白血病抑制因子(LIF)等细胞信号分子就能够在无喂养层的培养基上培养胚胎干细胞。
分离、鉴定与培养
胚胎干细胞的分离与培养
分离囊胚的内细胞群(ICM)细胞,再进行体外培养即可取得胚胎干细胞。目前,取得胚胎干细胞的方法已有一定改进,但仍无可避免地会杀死胚胎。
囊胚由两大部分构成:处于外围的滋养层以及处于内部的内细胞群。滋养层细胞会分化为胚胎外的组织(胎盘等),而内细胞群则会分化为胚胎的各种结构。
最早期分离胚胎干细胞的方法是先用蛋白酶分解透明带的蛋白质(囊胚外围的一层细胞外基质),再利用免疫手术(immunosurgery)专一地使滋养层细胞裂解,从而取得内部的内细胞群细胞,之后体外培养和繁殖取得的内细胞群细胞,即可建立胚胎干细胞系。目前胚胎干细胞的分离方法已有了一定的改进,比如现在已有使用激光去除透明带的技术。
获取胚胎干细胞的成功率相当低,即使成功取得胚胎干细胞,维持其不分化的状态也十分困难。为了阻止胚胎干细胞在培养过程中分化,培养基需加入如白血病抑制因子(LIF)等因子。最初,胚胎干细胞需要在含有喂养层细胞的培养基上培养。喂养层细胞能为胚胎干细胞提供特定的微环境,以抑制胚胎干细胞的分化。喂养层细胞常常使用经过有丝分裂阻断剂(如丝裂霉素)处理过的胚胎成纤维细胞。目前已能在成分清楚、无异物、不含有血清以及喂养层细胞的培养基上培养胚胎干细胞。
胚胎干细胞的鉴定
胚胎干细胞可以通过细胞集落或细胞本身的形态初步鉴定;除此之外,还可以从分子标记和分化潜能等两方面对胚胎干细胞进行鉴定。
各基因的表达情况随细胞不同而异。因此,可以用一些在细胞中特异性表达的蛋白质对胚胎干细胞进行鉴定。上述特异性表达的蛋白质又分为两种类型:细胞内的蛋白质以及细胞表面特异性的蛋白质(细胞表面标记)。目前较常用的细胞表面标记有SSEA-3、SSEA-4、TRA-1-60和TRA-1-81(前两者为阶段特异性胚胎表面抗原,后两者为肿瘤识别抗原);而常选为分子标记的细胞内蛋白质则有Oct4和Nanog等。免疫组织化学技术利用能与这些分子标记特异性结合的抗体来鉴定胚胎干细胞,此外,这种技术也能与流式细胞分选术、免疫磁珠等方法结合,用于胚胎干细胞的分离。
特异性分子标记的筛选可以采用转录组学与蛋白质组学的技术,将胚胎干细胞与其他细胞比对,以筛选出在胚胎干细胞中特异性表达的蛋白质。。
检验分化潜能也可以达到鉴定胚胎干细胞的目的。例如将小鼠的胚胎干细胞注射入其他的小鼠胚胎中,再使这个胚胎发育为完整个体,如果注射的胚胎干细胞具有多能性,最后就能形成嵌合体(即该小鼠的一部分细胞基因型与其他部分不同,该部分细胞来自注射的胚胎干细胞)。但是,考量伦理等方面的议题,上述方法并不适用于人类等动物。鉴定人胚胎干细胞的分化潜能主要有两种方法:体外培养形成拟胚体(embryoid body,EB)或注射入小鼠体内形成畸胎瘤。在体外低黏附性培养皿上培养人胚胎干细胞(或者悬浮培养人胚胎干细胞)能使胚胎干细胞形成一种特殊的结构,称为拟胚体,形成拟胚体的胚胎干细胞会分化为三大类分别具有外胚层、中胚层、内胚层细胞特征的细胞,利用不同的分子标记即可鉴定这三个胚层的细胞。如果将人胚胎干细胞注射入小鼠体内,则可以观察到畸胎瘤的形成,畸胎瘤的一些特征与早期胚胎相似,含有三大类分别具外胚层、中胚层、内胚层细胞特征的细胞。
复制本文链接 文章为作者独立观点不代表本网站立场,未经允许不得转载。

 京公网安备
11010802036058号
京公网安备
11010802036058号
评论