自噬(英语:Autophagy,或称自体吞噬)是一个涉及到细胞自身结构通过溶酶体机制,负责将受损的细胞器、错误折叠的蛋白及其他大分子物质等运送至溶酶体降解并再利用的进化保守过程。自噬是广泛存在于真核细胞的现象,并且可分为巨自噬、微自噬和分子伴侣介导的自噬三大类。这是一个受到紧密调控的步骤,此步骤是细胞生长、发育与稳态中的常规步骤,帮助细胞产物在合成、降解以及接下来的循环中保持一个平衡状态。目前已有多份研究表明自噬在许多细胞的分化进程中被不同程度地触发,例如参与血管生成、成骨分化、脂肪生成、神经发生等过程。
自噬效应的发生取决于自噬流过程是否完成,而自噬流的意思是自噬的完整动态过程,包括自噬体形成、自噬体与溶酶体融合及后续内含物的降解和回收。
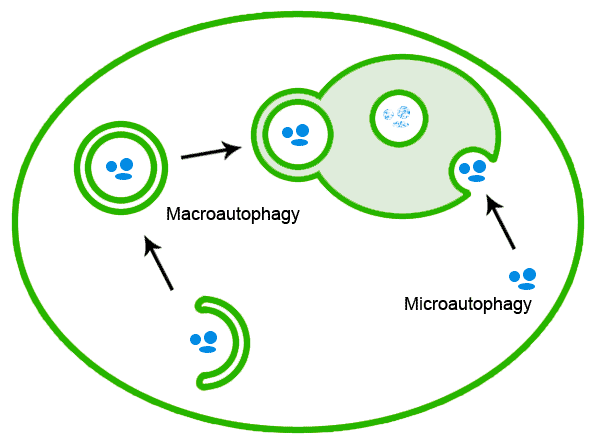
巨自噬与微自噬作用过程的对比
命名为“自噬”(英语:Autophagy)是由比利时化学家克里斯汀·德·迪夫在1963年发现的。当代的自噬研究是1990年代酵母的研究人员通过识别的自噬相关基因而被推动。其中之一人,日本科学家大隅良典因“对细胞自噬机制的发现”获得2016年度的诺贝尔生理学或医学奖。
分子生物学
属于丝氨酸/苏氨酸类蛋白激酶的ATG1/ULK1是启动自噬作用的关键蛋白激酶。自噬的初始阶段主要是诱导自噬和形成自噬膜,然而自噬膜的形成需要自噬前体(即自噬调控的重要节点)的形成。Beclin1-Vps34复合体是哺乳动物自噬的核心复合物。AtG4参与自噬泡的形成,而UVRAG作用于自噬泡成熟及其运输过程,Rubicon负调节其功能。诱导自噬后,在Atg14-Vps15-mVps34复合物作用下,启动膜泡的成核反应,进一步结合Atg21和Atg24,形成前自噬体。
自噬膜泡进一步扩张并包绕底物,最终形成自噬体。Atg12-Atg5复合物系统和LC3-Ⅱ-磷脂酰乙醇胺复合物系统均是泛素化系统,参与着自噬体的形成。目前已知p62蛋白会诱导镶嵌有LC3的自噬体到溶酶体,将其吞噬并清除,与底物结合的p62也能被蛋白水解酶降解,而细胞内的微管骨架其实也会将自噬体运输到溶酶体,水解酶在二者融合降解自噬体内容物,Rab7及UVRAG等因子参与此过程。目前已知Rab7与膜泡表面的脂分子尾部作用进行定位,而UVRAG则活化Rab7,将囊泡运送到靶位点。
自噬过程通常涉及两种泛素样偶联反应,以维持吞噬体的扩展。第1种反应发生在LC3 (酵母Atg8在哺乳动物中的同源物),LC3对溶酶体的形成是必需的。Atg4切割LC3获得弥散胞质状态的LC3-Ⅰ,LC3-Ⅰ其后与磷脂酰乙醇胺偶联,以形成膜结合状态的LC3-Ⅱ,LC3-Ⅱ其后定位于自噬体膜。Atg5-Atg12-Atg16L1复合物与前自噬体膜相关联,通过协助招募LC3延长它们的伸长。随着吞噬细胞扩大并接近闭合,Atg5-Atg12-Atg16L1复合物从外膜解离,而LC3-Ⅱ仍然与完成的自噬体结合。除此之外,mAtg9是核心Atg蛋白中唯一确定的多次跨膜蛋白,吞噬细胞的延伸也由mAtg9辅助。第2种反应则是在Atg12与Atg5共轭后,Atg16L1与偶联物Atg12-Atg5结合,形成一个对吞噬细胞成熟至关重要的Atg5-Atg12-Atg16L1复合物。
ATG8酯化在自噬发生过程中的作用仍未解释清楚,可以对促进自噬体膜的延伸和闭合起著关键作用。ATG8的酯化过程依赖于两个类泛素化系统的帮助。所有生物中的ATG5-ATG12共价结合复合物对于细胞内ATG8的酯化均是必须的。
在自噬相关基因中,Beclin1、Atg5、Atg12和LC3对自噬的诱导阶段十分重要。其中,LC3是自噬的关键蛋白,LC3前体正常会被ATG4切掉C端120个氨基酸,而残片称为LC3Ⅰ。胞膜形式的LC3Ⅰ在自噬发生时,已活化的LC3-Ⅰ经Atg3泛素化修饰后,与自噬泡膜表面的磷脂酰乙醇胺结合,形成自噬体膜形式且疏水性较强的LC3Ⅱ,并且铆钉于自噬泡双层膜结构上,参与细胞自噬。
ULK复合物对自噬诱导起始至关重要,主要由ULK1/2、自噬相关基因13(ATG13)、ATG101和200 kD家族相互作用蛋白组成。ULK1/2负责募集ATG蛋白,其中ULK1是哺乳动物自噬泡形成所必需的一种蛋白质,其活性缺失时LC3-Ⅱ不能形成,阻碍自噬过程。ULK1激酶复合体能够促进PI3K和ATG14形成复合物,并且促进Beclin1从Bcl2-Beclin1复合体中解离出来,形成参与自噬体核形成的关键因子Beclin1-PI3K-ATG14复合物。单磷酸腺苷活化蛋白质激酶(AMPK)和mTOR都可以催化ULK1的磷酸化 。AMPK在营养充足的条件下失活,mTORC活化并磷酸化ULK1和ATG13,从而抑制自噬起始。AMPK在饥饿条件下活化,同时mTORC失活,已活化的AMPK催化ULK1丝氨酸磷酸化,促进自噬作用。除此之外,ATG13可以由mTORC1磷酸化并调控ULK复合物的活性,ATG101结合并稳定FIP200,而FIP200则为ULK及ATG13提供支架。
PI3K复合物由Vps34、Vps15、Beclin1和Atg14蛋白组成,ULK1复合物在膜泡形成后会从由细胞质转移至内质网,并且增强PI3K复合物的活性,随后可产生磷脂酰肌醇-3磷酸酯,促进其他效应蛋白与自噬体膜结合,从而启动膜泡的成核反应,继而介导前自噬体的形成。
功能
营养不足
自噬在各种细胞功能中都发挥作用。营养不足会导致高水平的自噬,降解不需要的蛋白质,并且回收氨基酸,以合成对细胞生存至关重要的蛋白质。在高等真核生物中,自噬作用因动物在出生后切断了来自胎盘的食物供应而被响应。自噬能力降低的突变酵母细胞会在营养缺乏的情况下迅速消失。对APG突变体的研究表明,在饥饿条件下,通过自噬体进行的自噬对于液泡中的蛋白质降解是必不可少的,并且酵母中至少有15个APG基因参与自噬。营养素介导的自噬涉及一种称为ATG7的基因,因为小鼠研究表明,APG7缺陷型小鼠有着饥饿引起的自噬。
异种吞噬
在微生物学中,异种吞噬是指感染性颗粒的自噬性降解。细胞自噬机制在先天免疫中发挥重要作用。结核杆菌等细胞内的病原体被靶向降解,当中的细胞机制和调控机制与靶向线粒体降解的机制相同 。这是内共生学说的进一步证据。尽管某些细菌会阻止吞噬体成熟为降解的细胞器,称为吞噬溶酶体,但是这个过程通常会导致由侵入性微生物带来的破坏。
感染
水疱性口炎病毒是由自噬体从胞质溶胶中吸收并转移到内体中,并且在那里通过TLR7检测单链核糖核酸。在类铎受体被激活后,细胞内信号级联反应就会开始,导致干扰素和其他抗病毒细胞因子的诱导。部分病毒和细菌破坏了自噬途径,以促进自身复制。半乳凝素8已经被鉴定为细胞内的“危险受体”,能够启动针对细胞内病原体的自噬。当半乳凝素8与受损的液泡结合时,它会募集CALCOCO2等自噬受体,导致自噬体的形成和细菌的降解 。
修复机制
自噬可以降解受损的细胞器、细胞膜和蛋白质,而抵制自噬作用被认为是造成受损细胞蓄积和衰老的其中一个主要原因。自噬和自噬调节剂参与溶酶体损伤的反应,通常由半乳凝素-3和半乳凝素-8等半乳凝素指导,半乳凝素-8负责募集TRIM16。和NDP52等受体,并直接影响mTOR和AMPK的活性,而mTOR和AMPK分别抑制和激活自噬作用
程序性细胞死亡
程序性细胞死亡(PCD)的其中一个机制与自噬小体的出现有关,并且依赖于自噬蛋白。这种细胞死亡形式最有可能与形态学上定义为自噬PCD(autophagic PCD)的过程相对应。其中一个问题,是步入死亡过程的细胞中,其自噬的活性是导致其死亡的原因,还是为了防止细胞死亡的一个尝试。迄今为止,形态学和组织化学研究并未证明自噬过程与细胞死亡之间存在因果关系。最近有论据认为,垂死细胞中的自噬活性可能是一种生存机制。对昆虫变态的研究表明,细胞经历了一种PCD形式,这种形式与其他形式截然不同。这些已被提议作为自噬作用使细胞死亡的例子 。最近的药理和生化研究表明,有助细胞生存或致死的自噬可以通过应激期间,尤其是病毒感染后,调控信号的类型和程度来区分 。然而尚未在病毒系统之外观察到这些发现。
复制本文链接 文章为作者独立观点不代表本网站立场,未经允许不得转载。

 京公网安备
11010802036058号
京公网安备
11010802036058号
评论