免疫治疗已成为继手术、放疗和化疗后,癌症的第四大治疗方法,是近年来应用研究和临床医学实践的最前沿研究领域。随着人们对NK细胞作用机制研究的不断深入,基于NK细胞的免疫疗法已应用于临床治疗癌症。与传统的治疗手段相比,NK细胞可治疗多种不同的癌症,因而备受关注。
自然杀伤(natural killer, NK)细胞是一类具有杀伤肿瘤细胞能力的天然免疫细胞,可通过细胞毒性和释放细胞因子等方式,抵抗病毒或肿瘤细胞的侵袭。作为人体重要的免疫细胞之一,NK细胞在监视肿瘤的过程中发挥至关重要的作用,并以一种与抗原无关的方式表现岀对异常细胞的强大杀伤能力。
1975年,Kiessling等人发现一类与淋巴细胞形态相似,但与T细胞和B细胞不同的,不需要预先刺激就能裂解肿瘤细胞的细胞,并且能直接通过表面受体识别病原菌,因此,将其命名为自然杀伤细胞。
01
NK细胞及其功能
NK细胞主要参与对病毒感染细胞、恶性转化的自体细胞或同种异体细胞的杀伤过程,同时,能快速响应病毒感染,参与抗肿瘤的免疫监视过程。NK细胞是人体抵抗病毒感染和肿瘤细胞的第一道防线,能非特异性地直接杀伤肿瘤细胞,是免疫系统中最重要组成部分。
根据细胞特征,人们通常将NK细胞分为CD56hrieh,CD16dira表型和 CD56dim,CD16+表型。前者通常不太成熟,但可分泌大量的细胞因子;而后者更成熟,占NK细胞总数的90%,其细胞毒性更大,具有杀伤溶解靶细胞的功能,是天然抗肿瘤免疫的重要效应细胞。
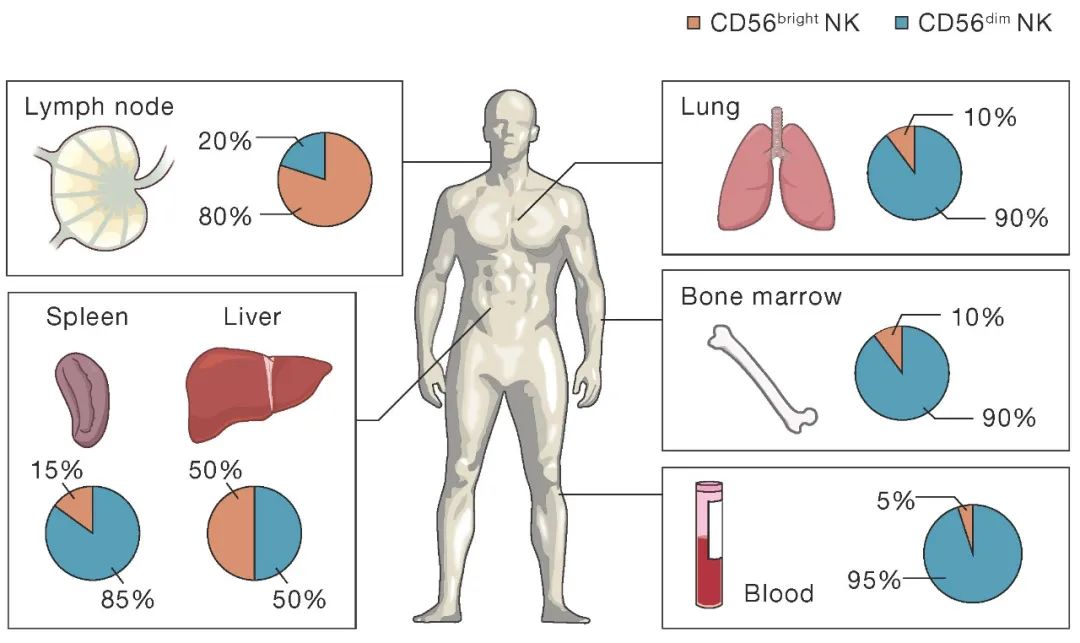
NK细胞及亚群在体内的分布。图片来源:Cell, doi: 10.1016/j.cell.2020.02.029
NK细胞的抗肿瘤作用依赖其细胞毒性,而细胞毒作用主要通过2种途径杀伤肿瘤细胞:
2)抗体依赖的细胞介导的细胞毒作用(antibodydependent cell—mediated cytotoxicity , ADCC )。
常规癌症治疗的“三板斧”分为:手术、放疗和化疗等.在这一过程中难免会使肿瘤细胞产生应激,增加NK细胞的活化配体,释放损伤相关分子模式分子(damage-associated molecular patterns molecules,DAMPs),诱导免疫原性的细胞死亡。
虽然不同化疗药物(或辐射)作用机制不同,但手术切除仍然是许多恶性实体瘤的主要治疗方法,而手术的免疫调节机制尚不清楚,同时手术在一定程度上影响了NK细胞的功能,可能为肿瘤的扩散和生长提供了机会。
02
癌症免疫治疗中
常见的NK细胞疗法
过继免疫治疗通过向肿瘤患者移植经体外诱导培养的、从患者或健康供者体内获得的、自体或异体的免疫细胞,发挥直接或间接地杀伤肿瘤细胞的作用,达到治疗肿瘤的目的。Rosenberg等人最早于1985年就开始使用NK细胞进行抗肿瘤治疗,研究发现,NK细胞联合IL-2对肾癌、黑色素瘤的治疗,有效率为20%~30%。

自体NK细胞
目前,自体NK细胞用于癌症免疫治疗,虽然NK细胞可从患者的外周血中分离,可在体外扩增,但部分研究显示,NK细胞的扩增比T细胞的扩增更为复杂。
自体NK细胞的功能状态和增殖往往较差,这可能与NK细胞分离前患者所接受的治疗有关,影响了临床疗效的原因之一。针对这一问题,目前正在研究多种方法包括不同的激活细胞因子组合(例如,IL-2 JL-12 JL-15 JL-18),体外扩增过程中使用饲养细胞提供重要的细胞因子等。
同种异体NK细胞
由于癌症患者的NK细胞功能高度失调.并且数量减少.因此,在癌症免疫治疗中,广泛探索了同种异体NK细胞的过继移植治疗,从而诱导产生抗肿瘤的效应。Miller等人在进行异体NK细胞回输的临床实验中发现,免疫抑制的AML患者回输NK细胞,并进行IL-2治疗后,IL-15升高、NK细胞数量增加,19名患者中有5名患者的疾病得到缓解:
诱导多能干细胞(induced pluripotent stem cells , iPSCs )也能分化为NK细胞,此种来源的NK细胞,无论在体内或体外,均证实对各种来源的肿瘤具有极高的细胞毒性。Zeng等人发现外周血iPSCs来源的NK细胞在体外人杀伤细胞免疫球蛋白样受体(killer cell immunoglohulin-like receptors , KIRs )的表达虽然较低,但对癌细胞同样具有细胞毒性,并可能产生ADCC,表明外周血iPSCs可能作为产生NK细胞的替代来源。
众多临床研究证实,同种异体NK细胞不会引起移植物抗宿主病(graft-versus-host disease ,GVHD),表明同种异体NK细胞的过继细胞治疗是安全的。与自体NK细胞过继细胞治疗相似,同种异体NK细胞过继细胞治疗体外培养的NK细胞扩增激活,回输体内后持续存在。
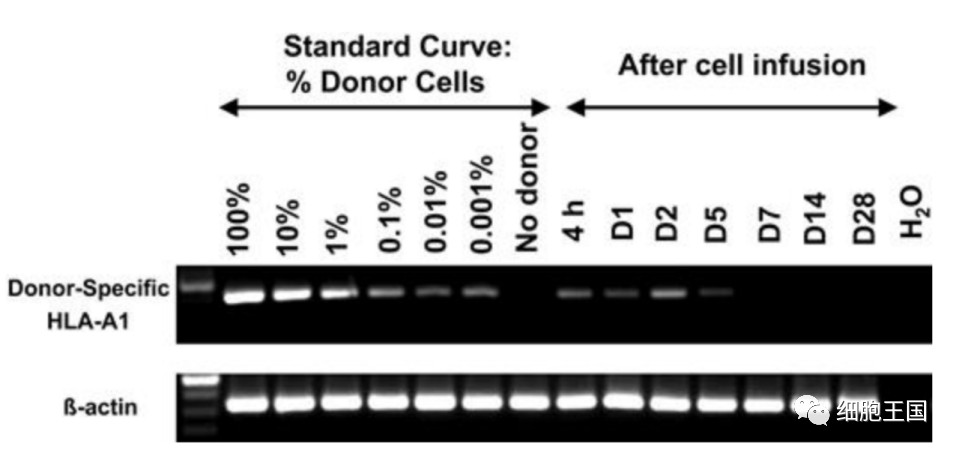
6名患者中有5名患者,供体细胞在体内持续存在 5 天。
来源:doi:10.1182/blood-2004-07-2974
03
嵌合抗原受体NK(CAR-NK)细胞
由于受NK细胞数量少、细胞毒性低和无法迁移至肿瘤部位等多种因素的影响,使未修饰的自体或异体NK细胞过继移植的临床应用受到限制。因此,对NK细胞进行基因工程修饰使其表达高亲和力受体(例如,CD16)、靶向表面蛋白(例如,PD-Ll.CD19.Her2等)和内源性细胞因子(例如,1L-2和IL-15)对NK细胞存活和细胞毒性至关重要。嵌合抗原受体技术是基因工程与免疫疗法的完美融合,在当前肿瘤治疗领域极具前景。
鉴于CAR-T细胞的成功,CAR现被用于增强NK细胞抗肿瘤活性。2005年,Imai等人利用基因修饰技术,将CAR-NK细胞表面克服了自身的抑制受体,开启了NK细胞基因修饰的先河。CAR-NK细胞不仅通过CAR特异性识别肿瘤表达的抗原,也可通过NK细胞自身受体清除肿瘤。
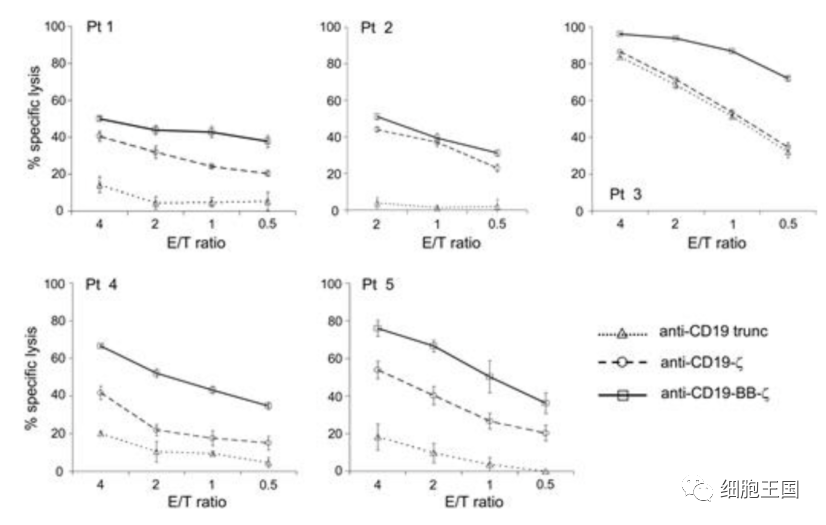
表达4-1BB增强嵌合受体的NK细胞对来自患者的白血病细胞表现出强大的细胞毒性。来源:https://doi.org/10.1182/blood-2004-12-4797
除了通过靶向肿瘤抗原指导CAR-NK细胞杀伤肿瘤细胞外,已有人提出CAR-NK细胞可清除肿瘤微环境中的免疫抑制细胞,包括骨髓源性抑制细胞(myelodi-derived suppressor cells, MDSCs)和M2型肿瘤相关巨噬细胞(tumor-associa-ted macrophages,TAMs)四。针对复发性或难治性CD19阳性B细胞恶性肿瘤患者的CD19靶向CAR-NK细胞治疗的I /II期临床试验(NCT03056339)中期结果显示,11例患者中有8例对治疗有客观反应,并未出现主要毒性反应。
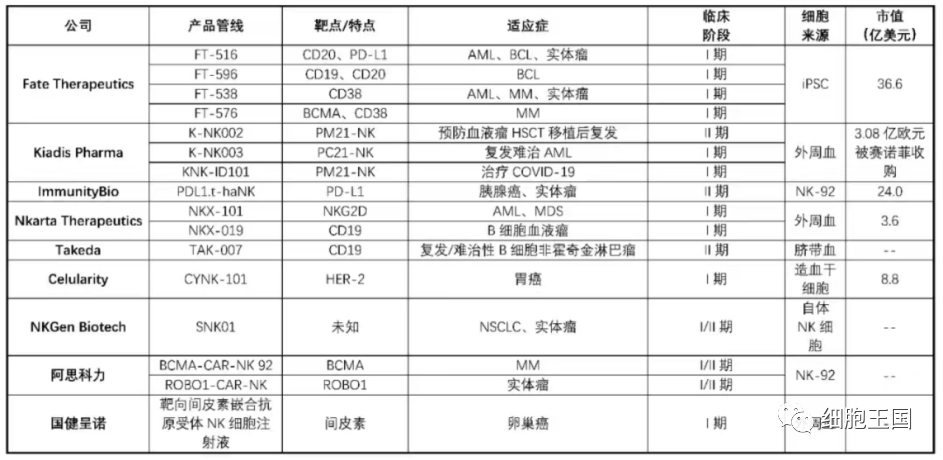
主要临床在研的CAR-NK产品
04
结语
作为一种具有快速、有效的抗肿瘤能力的特殊免疫表达细胞群,无论是否使用CAR,过继性NK细胞的移植均可提供一种更安全、更可行的替代方法,至少可作为基于T细胞治疗方法的补充。NK细胞易于获取、来源更多,使利用自体或异体NK细胞治疗疾病具有很大的潜力,特别是能增强免疫疗法的抗癌效果,并降低免疫治疗的毒性反应。
复制本文链接 文章为作者独立观点不代表本网站立场,未经允许不得转载。

 京公网安备
11010802036058号
京公网安备
11010802036058号
评论